Covid-19: Pfizer pede permissão aos EUA para imunizar crianças de 5 a 11 anos
Medida pode ajudar a proteger mais de 28 milhões de crianças estadunidenses
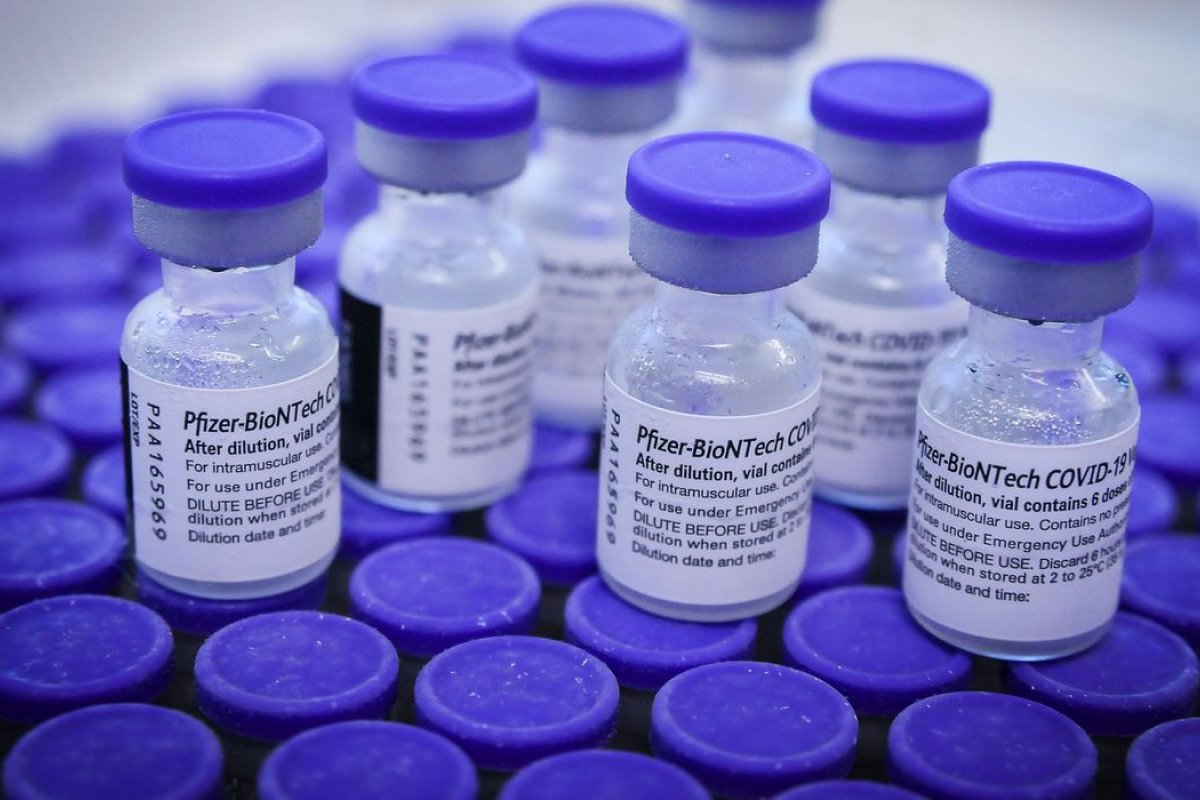
Foto: Geovana Albuquerque/ Agência Saúde - DF/ Agência Brasil
Na manhã desta quinta-feira (7), a Pfizer e a BioNTech disseram que pediram à Food and Drug Administration (FDA, órgão americano equivalente à Anvisa) que autorizasse o uso emergencial de sua vacina contra a Covid-19 em crianças de 5 a 11 anos. Se for aprovada, a medida pode ajudar a proteger mais de 28 milhões de crianças estadunidenses.
A FDA prometeu analisar com celeridade o pedido e agendou provisoriamente uma reunião em 26 de outubro para considerá-lo. Espera-se que uma decisão final saia até o fim de novembro.
Os pais se mostram animados com a possibilidade que afetará a vida de muitas famílias americanas.
A Dra. Janet Woodcock, uma comissária interina da FDA, disse na semana passada que as crianças podem exigir "uma dosagem ou diferente da usada em uma população pediátrica mais velha ou adultos", para a aplicação da vacina.
A Pfizer propôs um terço da dosagem adulta para as crianças. Isso pode exigir a adição de mais diluente a cada injeção ou o uso de um frasco ou série diferente. Esperava-se que a descrição da empresa sobre o método que pretende usar esteja em sua apresentação à FDA.


